電池は主に3つの構成要素で作られています。陰極、陽極、そしてこのふたつを物理的に分離する化学媒体である電解液です。
電池を電気回路や電球に接続すると、電解液の化学反応によって端末に電気が流れます。私たちが使っているさまざまなデバイスと同様に、電池は研究者たちの幾多の革新的な発見の賜物です。
”バッテリー(電池)”という言葉は1748年にベンジャミンフランクリンがライデン瓶について説明する際に初めて使われました。そして世界初の電池は1880年、アレッサンドロボルタが発表したボルタ電堆だといっていいでしょう。
私たちが今日使っている電池は大きさや化学組成などで分類できますが、一般的には再利用可能であると考えられています。
電池の形態には2つあり、それが以下のものです。
1.一次電池、または非充電式電池
2.二次電池、または充電式電池
一次電池、二次電池、合わせて10種類の電池をご紹介します。
一次電池
一次電池は使い切りの使用を目的として設計されています。この電池は化学反応を反転することができない電気化学セルでできているため、充電はできません。
世界の電池市場では一次電池が優位を占めていますが、一次電池は公衆衛生と環境に深刻な被害ををもたらすものでもあります。よく使われている一次電池のタイプについて説明します。
10.マンガン乾電池(亜鉛炭素電池)

放電容量:400−1700 mAh (ミリアンペアアワー)
電圧:1.5 V (ボルト)
マンガン電池では、亜鉛とマンガン酸化物の間の非可逆的電気化学反応により電気が発生します。この電池の外層は亜鉛で来ていて、次の層は塩化アンモニウム(電解質として作用)ですが、紙製のセパレーターによって二酸化マンガンと分けられています。
電池の中心は正極として働く炭素棒です。炭素棒は基本的に亜鉛と二酸化マンガン間の酸化還元反応で起きた発電電流を集めます。
二酸化マンガン電池は1866年に発明された湿電池、ルクランシェ電池から着想を得ています。1900年代初頭には二酸化マンガン電池は初の乾電池として商業的に売り出されました。二酸化マンガン電池は懐中電灯のような持ち運ぶも製品に使えるため人気が出ました。今日では主にラジオやリモコンなどに使われています。
塩化亜鉛電池により従来品の性能が大幅に向上しました。はるかに純粋な化学的配置のおかげで塩化亜鉛電池は、より長い使用年数でより安定した電圧を作りだすことができます。
9.原子力電池
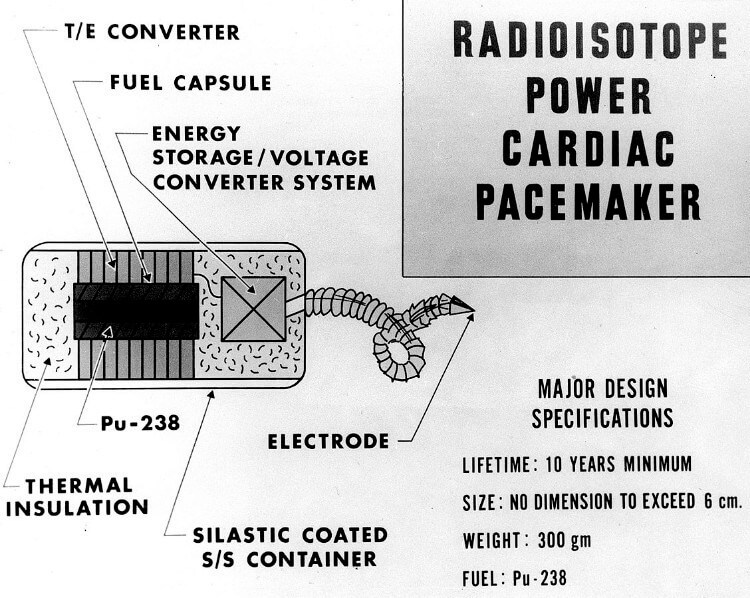
原子力電池は原子炉によく似た放射性崩壊のエネルギーを利用して電力を生みます。原子炉との違いは原子力電池は連鎖反応を使わないということです。予想できることですが、この電池は他の電池に比べると高額です。
しかし原子力電池は出力濃度が高く、心臓のペースメーカーや深海で使われる道具、航空機といった隔離された環境で長時間作動しなければならないものの使用に適しています。
原子力電池はエネルギー変換アプローチに基づいて熱性と非熱性の2つに広く分類されます。
放射性同位体熱電気転換器(RTG)と熱光起電力セルを含む熱変換器は温度差によって発電します。熱は原子力によって発生するもので、そのあとに発電に使用されます。
一方、ベータボルテックスのような非熱変換器は、トリチウムと呼ばれる水素同位体の崩壊中に生成される高エネルギー電子を捉えることによって電気を作ります。
最初の原子電池は1913年にヘンリーモーズリーによってラジウムを基盤してに開発されました。
8.酸化銀電池

電圧:1.55 V
酸化銀電池も一次電池の1つです。コスト面から、酸化銀電池は一般的に小さいサイズのボタン電池として売られています。しかしながら軍、または宇宙開発などコストがあまり問題にならず、質の良さが最大の問題となる限られた分野においては従来にないデザインの大型酸化銀電池が多数採用されています。
酸化銀電池はその寿命の長さから宇宙船の打ち上げに使用される車両や有人宇宙船、衛星などのために特に開発されました。ソビエト連邦のスプートニク衛星、アポロ月着陸船から第二次世界大戦中の魚雷まで、すべてこの電池から動力を得ていました。
これまで、何千もの研究が、酸化銀電池をより一般的なニーズに適応できるよう研究を進めています。
7.リチウム電池

電圧:1.5V – 3.7
リチウム電池という言葉はリチウム金属化学に基づく電池のグループの総称として使われます。複数の化学物質の組み合わせが共通物質てして金属リチウム(陽極として)と共につかわれます。最も広く使用されているリチウム電池は二酸化マンガンを陰極として、溶解したリチウム塩と共に使っています。
希少なリチウム電池としてリチウム塩化チオニル電池があります。これは1973年に発明されたものです。リチウム塩化チオニル電池は低・中程度のパワーエレクトロニクスに適していて、市販はほとんどされていません。
誤解を招きやすいのですが、リチウム電池はし充電式の電池であり、二次電池の中のリチウムイオン電池やリン酸電池とは別のものです。
リチウム電池は様々な形や大きさのものがありますが、コインタイプの電池が最も人気があります。カメラなどに使われている通常のアルカリ性乾電池の代わりにもなります。
一方、リチウム電池は様々な電池の中で最も環境にも人体にも脅威を及ぼすもので、メタンフェタミンの違法生産にも使われています。
6.ニッケル酸電池
ニッケル酸電池(二オックス電池)標準的なアルカリ電池とは若干異なります。亜鉛と二酸化マンガンだけをカソードに使う代わりにニッケル酸と黒鉛を混合物に加えてあります。
これによってニッケル酸電池は電池あたりの電圧を比較的高いものにすることができ、これによって電池で作動する端末を良好に作動させることができます。
高電圧出力は新しく改良された化学組成にだけ起因するものではなく、電解質を電池に充填する真空製造プロセスにも起因しています。しかしながら高電圧はトーチや懐中電灯のような発光電球を使っている器具においては不具合の原因になる可能性もあります。
電池の残りを調べるインジケーターが間違った電池の情報を示す場合もあります。
5.アルカリ電池

放電容量:1アンペア負荷で700mAh(標準サイズの電池)
電圧:1.5 V
アルカリ電池は世界的に広く使われている一次電池で、亜鉛と二酸化マンガン間の化学反応によって電気を生成しています。苛性カリとしても知られる水酸化カリウムを電解質として使っています。
アルカリ電解質を使っているその他の電池、特に充電式のアルカリ乾電池などはアルカリ電池とは異なる物質を電極に使用しています。このような電池は一般にデジタルカメラ、おもちゃ、ラジオ、MP3プレーヤーなどの簡単に持ち運べる機器に使われています。
アメリカで製造される電池の80%がアルカリ乾電池です。EU全体での割合は平均で47%で、スイスでは68%近く、イギリスでは60%です。2010年の統計では年間100億本以上のアルカリ電池が生産されています。
二次電池
一次電池とは異なり、二次電池は充電するとが可能で、何度放電しても使うことができます。
技術的には二次電池は電気化学反応を反転できる電池ということになります。二次電池には20以上の種類がありますが、最も認知度が高いものだけをご紹介します。
4.鉛酸電池

電圧: 2.1 V(定格)
環境に優しい省エネ電池の人気が出る以前は鉛酸電池が市場を牽引していました。フランスの物理学者ガストン・プラントが1859年に独自に発明した鉛酸電池が初期の電気自動車のバッテリーとして大ヒットしました。
フルチャージの鉛酸電池は、ゲル化した鉛を陰極と電解質に、二酸化鉛を陽極に、硫酸を電解質に使用しています。陰極からイオンが電解質に移動して陽極に吸収されるときに電気が生成されます。また充電時にはこれと反転の反応が起こります。
鉛酸電池は一般的に自動車産業においてイグニションや照明に用いられます。その他には電話塔やデータセンターの予備電力として使われています。潜水艦が完全に水中にいる状態の時の電力施設としても利用されます。
しかしながら、この電池は他の種類のものと比べると有害です。この何十年かの間、鉛酸電池から排出される有毒物質が世界中の環境団体からの注目を集めています。
3.ニッケルカドミウム蓄電池

電圧:1.2 V
もうひとつの充電可能な電池は、メタリックカドミウムと水酸化ニッケルを電極に、主に水酸化カリウムのアルカリ電解質を使っているニッケルカドミウム電池(ニカド電池)です。1899年、スウェーデン人発明家のウォルデマールジュングナーが鉛酸電池に代わるものとして発明しました。
ニッケルカドミウム電池はマンガン電池やアルカリ電池に比べて電圧が低いため(1.2V)多くの電気機器には不向きです。しかしながら他の電池とは違い、ニッケルカドミウム電池の電圧は放電時にわずかに劣化するに留まります。多くの持ち運び用の機器は定電圧で作動する設計になっています。(電池あたり0.90から1.0V)
ニッケルカドミウム電池はメモリーエフェクト(完全に放電する前に充電を繰り返すことで最大容量まで充電されなくなる現象)を被る可能性がある電池だということはあまり知られていません。
玩具産業で広く使われていて、かつては持ち運ぶ機器や電子装置、カメラや懐中電灯などに広く使用されていました。
2.ニッケル水素電池

電圧 : 1.2 V
ニッケル水素電池は基本的にはニッケルカドミウム電池をアップグレードさせたものです。どちらの電池も同じアルカリ電解質(水酸化カリウム)とニッケル水素を陽極に使っています。
唯一の違いはニッケル水素電池はカドミウムの代わりに水素イオンを陰極に使用しているという点です。これによってニッケル水素電池はにニッケルカドミウム電池の3倍容量を持つことができます。
多くの場合これらのエネルギー密度はリチウムイオン電池と同じぐらいのレベルに達します。ニッケル水素電池は一時ほとんどの国、特に家電製品において単三電池が使われているところではニッケルカドミウム電池に変わって普及しました。
また、耐久性が高く内部抵抗が低いため、ニッケル水素電池は標準的なアルカリ電池よりも優れています。リチウムイオン電池ほど一般的ではありませんが、様々な種類の電気自動車にも使われています。
⒈リチウムイオン電池

放電容量:3,000mAh (ミリアンペアアワー)
電圧:3.2 V (リン酸リチウム鉄), 3.6V – 3.7V
リチウムイオン電池の記録的な発展はその性能の高さ、全体としての安全性そして40年以上研究が続けられていることにあると考えられます。
スマートフォン、パソコン、タブレット、電気工具、自動車、ひいては様々な航空宇宙システム至るまで、ほとんどどこででも使われています。リチウムイオン電池は様々な形、サイズ、化学構造のものがあります。
高エネルギー密度の携帯電子機器に使われている、最も一般的なリチウムイオン電池のひとつは酸化コバルトリチウムをベースにしています。
その他のもの、例えばリチウムイオンマンガン酸化物や酸鉄リチウム電池といった電池はエネルギー密度は低いものの爆発しにくいのが特徴です。これらの電池は、電池自体が生成するよりわずかに高い電圧が付加される過電圧状態で充電されます。
充電の過程において電池内の電流は正極から負極に流れます。この流れは電池が放電する場合は逆の流れになります。


























